前言
在细胞治疗中,CAR识别表位对于免疫治疗效果有非常重要影响。目前CAR-T在实体瘤治疗中发展较为缓慢,B7-H3是一个新兴的CAR-T实体瘤治疗靶点,其胞外域包含两个不同的表位基序:IgC和IgV。本文介绍一项基于纳米抗体的B7-H3 CAR-T细胞治疗产品,该产品亮点是其中的中B7-H3纳米抗体识别IgC而非IgV表位而对小鼠实体瘤模型表现出更加有效的抗肿瘤活性。
4IgB7-H3是实体瘤中的主要亚型
人B7-H3包括两种亚型,2IgB7-H3 (2Ig)和4IgB7-H3 (4Ig)。检测转录本分析发现,B7-H3在各种肿瘤组织及细胞系中异常高表达,并与胰腺癌和神经母细胞瘤患者低的总生存期相关。而4IgB7-H3亚型是在胰腺癌和神经母细胞瘤等多种实体瘤类型中表达的主要亚型,且4Ig是高度糖基化的(图1),这也表明4IgB7-H3亚型可以作为癌症免疫治疗的泛癌靶点。
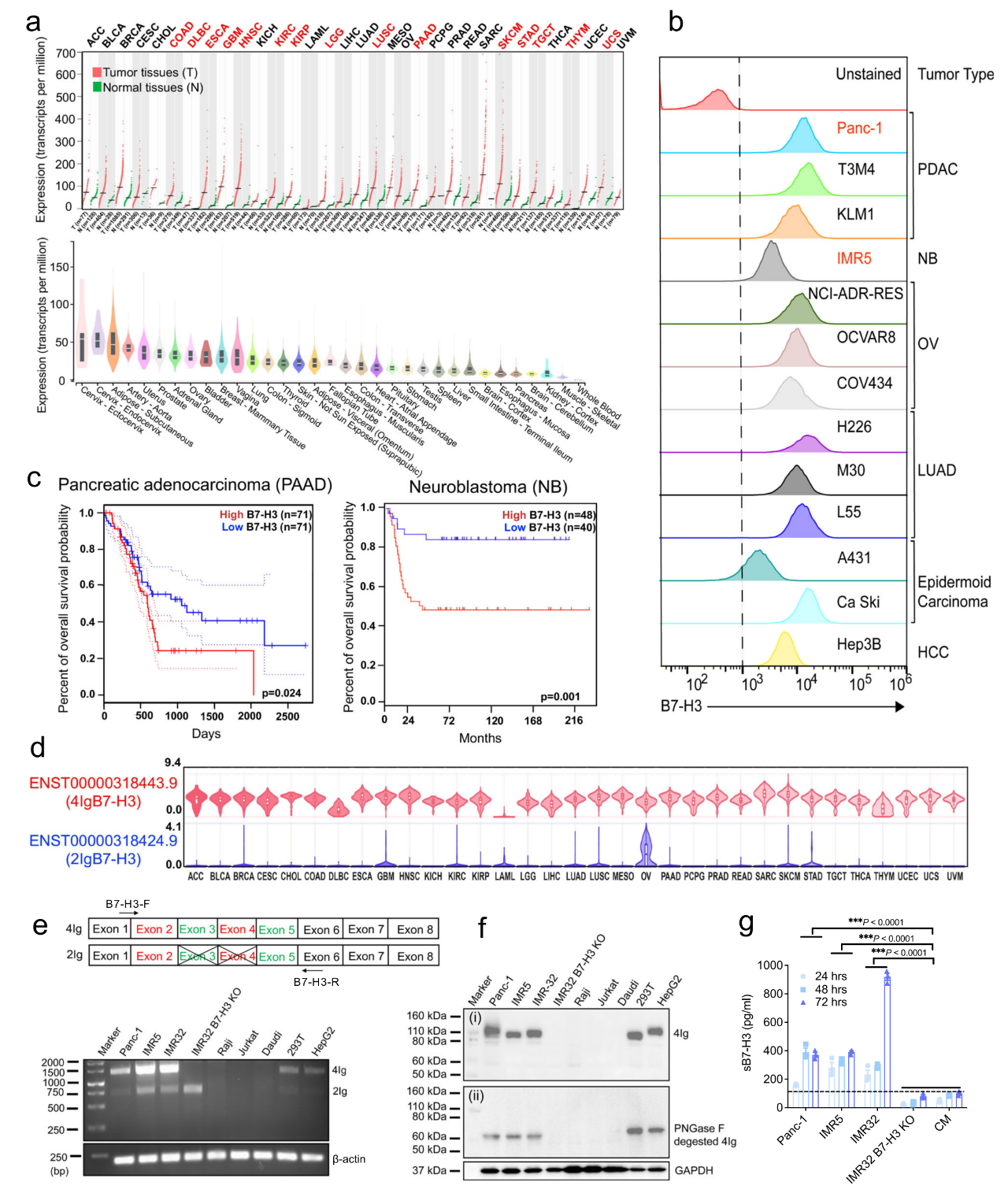
图1. 4IgB7-H3在多种实体癌中高度过表达
靶向B7-H3纳米抗体开发
使用噬菌体展示技术从8个单峰骆驼VHH纳米抗体库((>1E12 pfu/ml total) 中筛选出针对4IgB7-H3的纳米抗体。获得10个克隆与人4IgB7-H3蛋白结合,通过ELISA、动力学抗体结合、WB和流式细胞术技术检测发现,其中高亲和力的纳米抗体C4、B12和G8与肿瘤细胞上表达的天然4IgB7-H3结合(图2)。
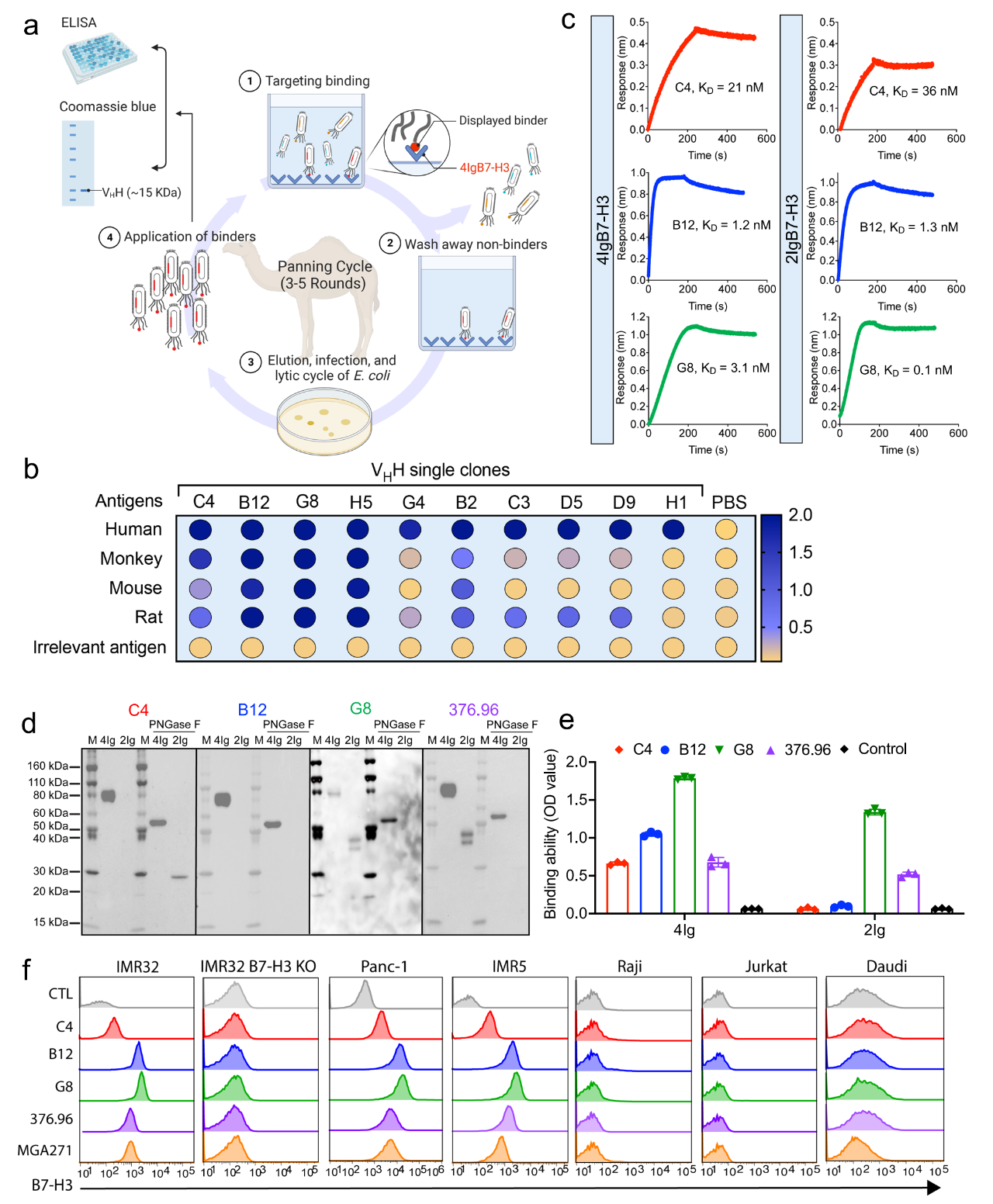
图2 4IgB7-H3高亲和力纳米抗体开发
靶向B7-H3纳米抗体识别表位鉴定
通过在Octet平台上进行4IgB7-H3抗原的交叉竞争测定发现,G8和已知的抗B7-H3的单克隆抗体376.96在4IgB7-H3的IgV结构域具有重叠表位。通过研究从哺乳动物细胞中纯化的抗原片段与VHH-Fc的相互作用,发现B12和C4与4IgB7-H3 IgC结构域的不同区域结合(图3)。
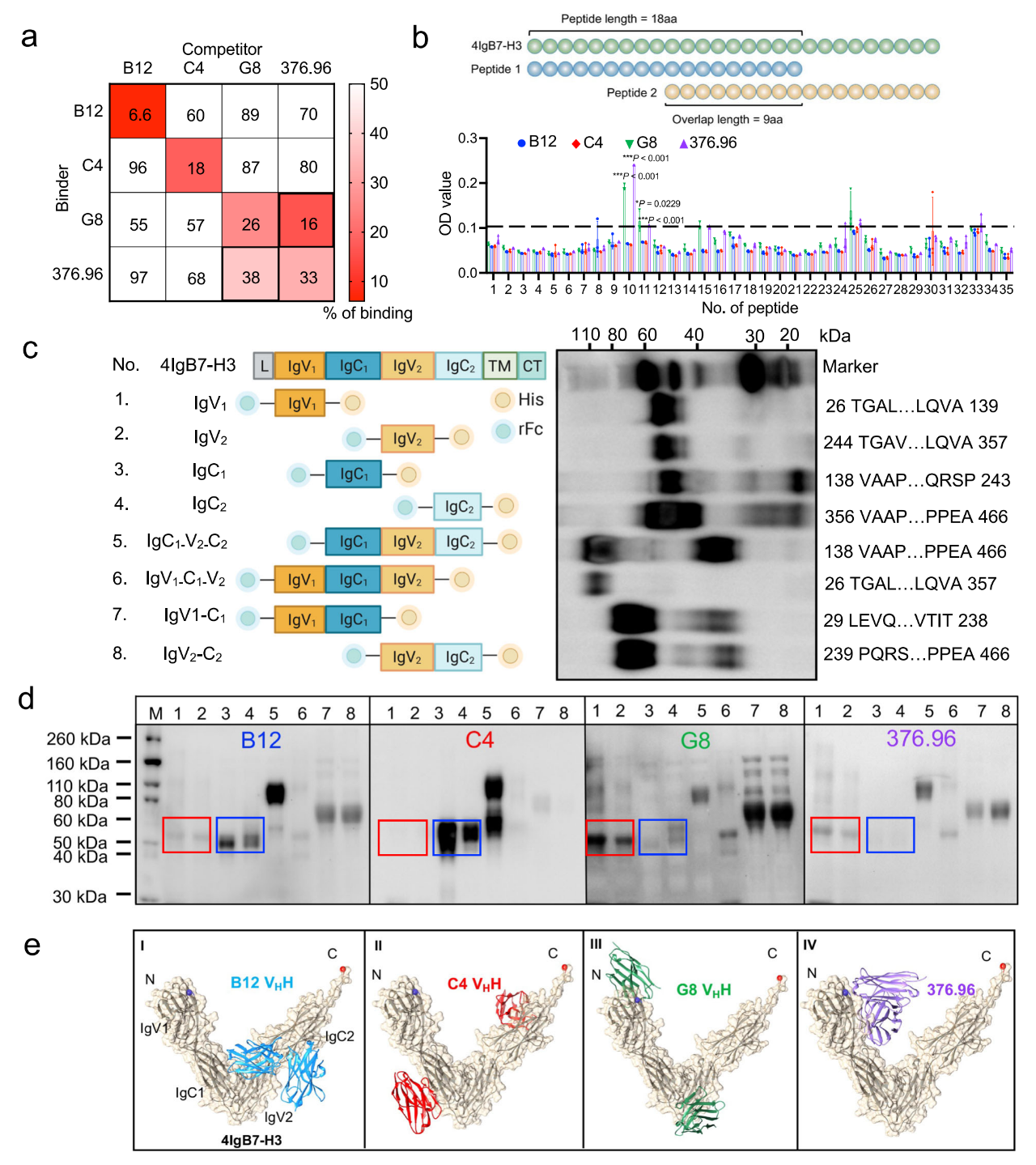
图3 抗B7-H3纳米抗体的表位预测
基于B7-H3纳米抗体的CAR-T细胞在体外杀伤人胰腺癌和神经母细胞瘤细胞
将单个VHH片段插入到临床上使用的CAR载体中来生成B7-H3 CAR-T细胞,而后将其与肿瘤细胞系共孵育,发现它以抗原依赖的方式显著杀伤胰腺癌(Panc-1)和神经母细胞瘤细胞系(IMR32、IMR5)。尽管基于纳米抗体的CAR-T细胞和基于376.96 scFv的CAR-T细胞对IMR5肿瘤细胞具有相当的细胞毒性,但B12(VHH)-CAR-T细胞释放的细胞因子(IFN-γ、IL-2和TNF-α)水平明显更高。抗原结合能力和抗体阻断实验表明,B12(VHH)-CAR-T细胞具有更高的抗原结合能力,且天然4IgB7-H3抗原参与细胞功能的激活。通过CAR-Jurkat NF-κB和NFAT报告细胞系评估发现B12(VHH)-CAR激活活性最强,可能的原因是因为其更强的抗原结合能力(图4)。

图4 基于B7-H3纳米抗体的CAR-T细胞在体外有效杀伤胰腺癌和神经母细胞瘤细胞
基于B7-H3纳米抗体的CAR-T细胞根除小鼠胰腺癌
为了临床前评估基于B7-H3纳米抗体的CAR-T细胞的抗肿瘤功效,在20天后向Panc-1转移异种移植小鼠模型单次注射250-1000万个CAR-T细胞,发现B12(VHH)-CAR-T细胞和C4(VHH)-CAR-T均能显着消除肿瘤负荷。治疗后再次激发肿瘤,发现肿瘤快速缩小,表明小鼠体内已具有持久性的CAR-T活性。在250万个CAR-T细胞剂量下,发现靶向B7-H3 IgC结构域的B12(VHH)-CAR-T和C4(VHH)-CAR-T细胞相较于靶向B7-H3 IgV的376.96(scFv)-CAR-T和G8(VHH)-CAR-T细胞对Panc-1保持了更高的抗肿瘤疗效,从而延长小鼠生存时间。类似的,250万个B12(VHH)-CAR-T细胞可以显著消退原位胰腺癌小鼠模型中的Panc-1原位肿瘤(图5)。

图5 基于B7-H3纳米抗体的CAR-T细胞在小鼠中对人胰腺癌抗肿瘤活性
B12(VHH)-CAR-T细胞对小鼠转移性和大实体瘤具有最强的抗肿瘤活性
研究发现B12(VHH)-CAR-T细胞通过介导肿瘤细胞杀伤,对小鼠模型中的IMR5转移性神经母细胞瘤、大至400-800 mm3的NBEB神经母细胞瘤异种移植瘤和大至250 mm3的BxPC-3胰腺癌异种移植瘤均表现出显著的肿瘤生长抑制,且这种抑制是B7-H3靶向性的。而C4(VHH)-CAR-T和376.96(scFv)-CAR-T细胞仅显示出有限的疗效(图6)。
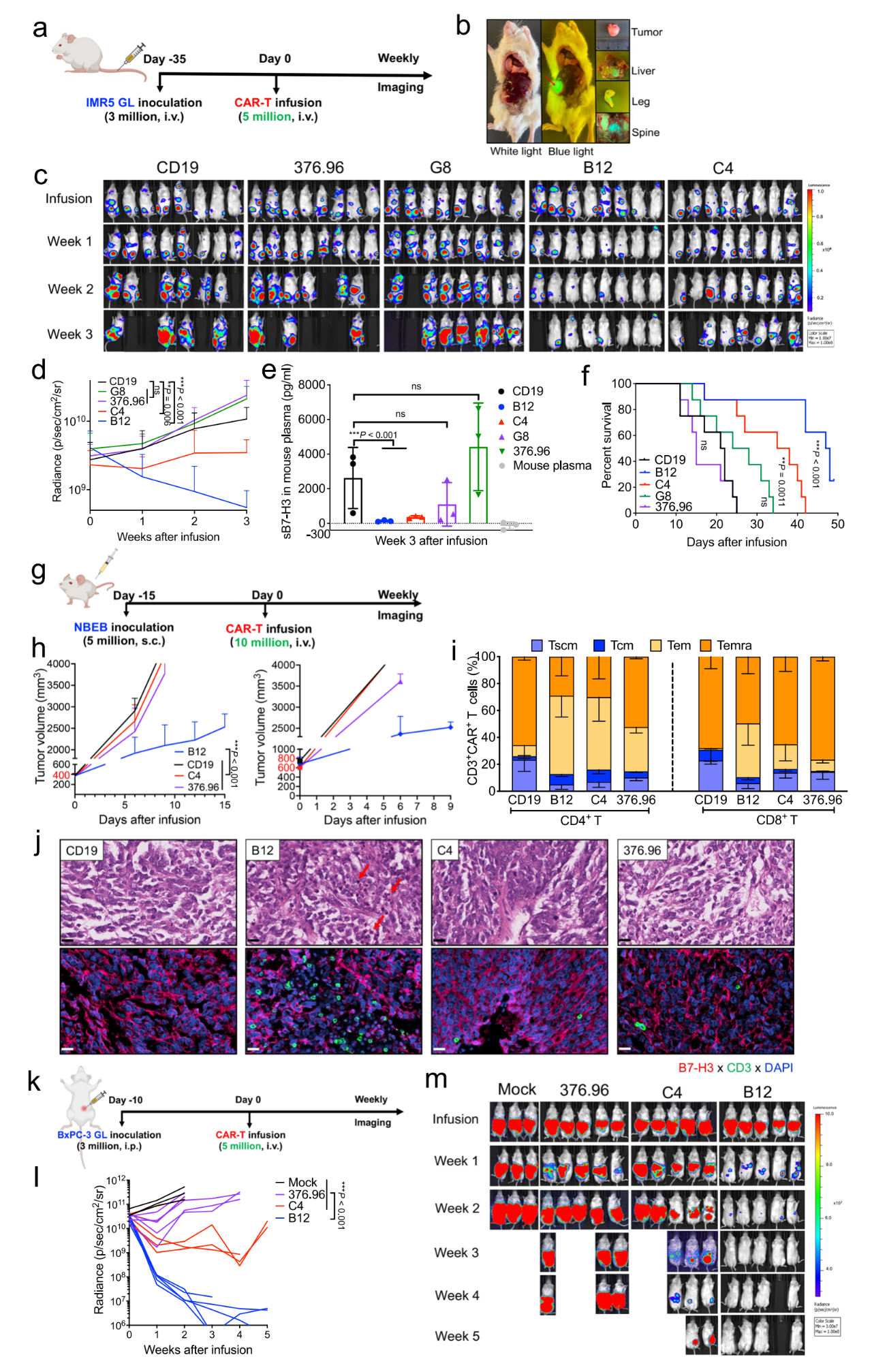
图6 B12(VHH)-CAR-T细胞抑制异种移植中转移性和大型肿瘤生长
小结
B7-H3在各种实体瘤中异常过表达,其4IgB7-H3亚型作为常见亚型,是开发免疫治疗的潜在靶点。本研究报道的靶向B7-H3的纳米抗体可以与4Ig和2Ig蛋白结合,其中基于B12 (VHH)的CAR-T细胞识别4IgB7-H3 IgC结构域中的独特表位,对小鼠晚期转移性和大型实体肿瘤具有良好的抗肿瘤作用。这项研究证明了基于VHH的CAR-T细胞治疗包括胰腺癌和神经母细胞瘤在内的实体瘤的潜力,并为在CAR-T细胞治疗中CAR识别表位影响提供一种解决策略。
阿帕克生物基于可分泌酵母展示技术平台,提供一站式纳米抗体研发服务,欢迎合作交流!
参考文献:
Li, D., Wang, R., Liang, T. et al. Camel nanobody-based B7-H3 CAR-T cells show high efficacy against large solid tumours. Nat Commun 14, 5920 (2023). doi: https://doi.org/10.1038/s41467-023-41631-w
了解更多纳米抗体相关内容,可关注<阿帕克生物>微信公众号,获取最新资讯~
